百科详情
发布时间:2024-08-01 19:20

1简介
 亮氨酸 (Leu,L)
亮氨酸 (Leu,L)
拼音名:Liang’ansuan
英文名:Leucine
书页号:2000年版二部-525
化学式:C6H13NO2 131.17
分子式:(CH3)2CHCH2CH(NH2)COOH
本品为L-2-氨基-4- 甲基戊酸。按干燥品计算,含C6H13NO2不得少于98.5%。
【性状】 本品为白色结晶或结晶性粉末;无臭,味微苦。
本品在甲酸中易溶,在水中略溶,在乙醇或乙醚中极微溶解。
比旋度 取本品,精密称定,加6mol/L盐酸溶液溶解并释稀成每1ml 中含40mg的溶液,依法测定(附录Ⅵ E),比旋度为+14.5°至+16.0°。
【鉴别】 本品的红外光吸收图谱应与对照的图谱(光谱集298 图)一致。
2检查
酸度 取本品0.50g ,加水50ml,加热使溶解,放冷至室温,依法测定(附录Ⅵ H),pH值应为5.5 ~6.5 。
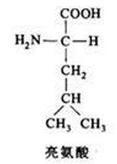 结构式 溶液的透光度 取本品0.50g ,加水50ml,加热使溶解,放冷至室温,照分光光度法(附录Ⅳ A),在430nm 的波长处测定透光率,不得低于98.0%。
结构式 溶液的透光度 取本品0.50g ,加水50ml,加热使溶解,放冷至室温,照分光光度法(附录Ⅳ A),在430nm 的波长处测定透光率,不得低于98.0%。
氯化物 取本品0.25g ,依法检查(附录Ⅷ A),与标准氯化钠溶液5.0ml 制成的对照液比较,不得更浓(0.02%)。
硫酸盐 取本品1.0g,依法检查(附录Ⅷ B),与标准硫酸钾溶液2.0ml 制成的对照液比较,不得更浓(0.02%)。
铵盐 取本品0.10g ,依法检查(附录Ⅷ K),与标准氯化铵溶液2.0ml 制成的对照液比较,不得更浓(0.02%)。
其他氨基酸 取本品,加水制成每1ml 中含4mg 的溶液,作为供试品溶液;精密量取上述溶液适量,加水释稀成每1ml 中含20μg 的溶液,作为对照溶液。照薄层色谱法(附录Ⅴ B)试验,吸取上述两种溶液各5μl ,分别点于同一硅胶G薄层板上,以正丁醇-水-冰醋酸(3:1:1 )为展开剂,展开后,晾干,喷以茚三酮的丙酮溶液(1 →50),在80℃干燥5 分钟,立即检视,供试品溶液所显杂质斑点的颜色,与对照溶液的主斑点比较,不得更深(0.5 %)。
干燥失重 取本品,在105 ℃干燥3 小时,减失重量不得过0.2 %(附录Ⅷ L)。
炽灼残渣 取本品1.0g,依法检查(附录Ⅷ N),遗留残渣不得过0.1 %。 铁盐 取本品1.5g ,依法检查(附录Ⅷ G),与标准铁溶液1.5ml 制成的对照液比较,不得更深(0.001%)。
重金属 炽灼残渣项下遗留的残渣,依法检查(附录Ⅷ H第二法),含重金属不得过百万分之十。
砷盐 取本品2.0g,加水5ml,加硫酸1ml与亚硫酸10ml,在水浴上加热至体积约剩2ml ,加水5ml,滴加氨试液至对酚酞指示液显中性,加盐酸5ml ,加水使成28ml,依法检查(附录Ⅷ J第一法),应符合规定(0.0001%)。
热原 取本品,加氯化钠注射液制成每1ml中含20mg的溶液,依法检查(附录Ⅺ D),剂量按家兔体重每1kg 注射10ml,应符合规定(供注射用)。
【含量测定】 取本品约0.1g,精密称定,加无水甲酸1ml 溶解后,加冰醋酸25ml,照电位滴定法(附录Ⅶ A),用高氯酸滴定液(0.1mol/L)滴定,并将滴定的结果用空白试验校正。每1ml高氯酸滴定液(0.1mol/L)相当于13.12mg的C6H13NO2。
【类别】 氨基酸类药。
【贮藏】 遮光,密封保存。
用 途:营养增补剂;调味增香剂。
配制氨基酸输液及综合氨基酸制剂,降血糖剂,植物生长促进剂。
3实验室测定方法
方法名称: 亮氨酸测定—电位滴定法
应用范围: 本方法采用滴定法测定亮氨酸的含量。
本方法适用于亮氨酸 。
方法原理: 供试品置锥形瓶中,加无水甲酸与冰醋酸溶解后,照电位滴定法,用高氯酸滴定液(0.1mol/L)滴定。读出高氯酸滴定液使用量,计算亮氨酸的含量。
试剂: 1. 水(新沸放置至室温)
2.高氯酸滴定液(0.1mol/L)
3. 结晶紫指示液
4. 无水甲酸
5 .冰醋酸
6. 基准邻苯二甲酸氢钾
仪器设备:
试样制备: 1.高氯酸滴定液(0.1mol/L)
配制:取无水冰醋酸(按含水量计算,每1g水加醋酐5.22mL)750mL,加入高氯酸(70%-72%)8.5mL,摇匀,在室温下缓缓滴加醋酐23mL,边加边摇,加完后再振摇均匀,放冷,加无水冰醋酸适量使成1000mL,摇匀,放置24小时。若所测供试品易乙酰化,则须用水份测定法测定本页的含水量,再用水和醋酐调节至本液的含水量为0.01%-0.2%。
标定:取在105℃干燥至恒重的基准邻苯二甲酸氢钾约0.16g,精密称定,加无水冰醋酸20mL使溶解,加结晶紫指示液1滴,用本液缓缓滴定至蓝色,并将滴定的结果用空白试验校正。每1mL高氯酸滴定液(0.1mol/L)相当于20.42mg的邻苯二甲酸氢钾。根据本液的消耗量与邻苯二甲酸氢钾的取用量,算出本液的浓度,即可。
贮藏:置棕色玻璃瓶中,密闭保存。
2. 结晶紫指示液
取结晶紫0.5g,加冰醋酸100mL使溶解,即得。
操作步骤: 精密称取供试品约0.1g,置锥形瓶中,加无水甲酸1mL溶解后,加冰醋酸25mL,照电位滴定法,用高氯酸滴定液(0.1mol/L)滴定,并将滴定结果用空白试验校正。记录消耗高氯酸滴定液的体积数(mL),每1mL高氯酸滴定液(0.1mol/L)相当于13.12mg的C6H13NO2。
注1:“精密称取”系指称取重量应准确至所称取重量的千分之一,“精密量取”系指量取体积的准确度应符合国家标准中对该体积移液管的精度要求。
参考文献: 中华人民共和国药典,国家药典委员会编,化学工业出版社,2005年版,二部,p.445。
4生产方法
氨基酸的制造是从1820年水解蛋白质开始的。1908年日本人Ikeda发现谷氨酸钠是鲜味的强化剂,开始了工业化生产氨基酸的历史。1957年日本开始运用微生物进行谷氨酸发酵生产,从此揭开了微生物发酵方法生产氨基酸的历史新篇章。20世纪六十年代左右,关于L一亮氨酸生物合成以及其代谢调节机制相继阐明。这为微生物发酵法生产L一亮氨酸定向育种及酶法生产L-亮氨酸提供了理论基础。
L一亮氨酸的生产方法主要有提取法、化学合成法、酶催化法、微生物发酵法等。
蛋白质水解法
氨基酸是蛋白质的组成单位,在酸性条件下,将L一亮氨酸含里较高的蛋白质水解,得到各种氨基酸的混合物,经分离、纯化、精致等工序获得L一亮氨酸产品。
我国大部分厂家采用蛋白质水解法生产L一亮氨酸和L-胱氨酸。蛋白质水解法生产L一亮氨酸的优点是生产设备简单,技术要求不高,并且L一亮氨酸在蛋白质中的含量较高。但是蛋白质水解法生产的缺点是费时、污染严重、收率低、产品质量得不到保证,大规模生产受到限制。
化学合成法
亮氨酸化学合成法有A.Strecker, n一卤代酸氨解、相转移催化等几种方法。虽然化学合成法原理简单,价格低廉,但操作复杂,反应条件苛刻,副产物多,产率不高,并且有的方法涉及到有毒物质。化学合成法得到亮氨酸是消旋的DL一亮氨酸,为了得到L一亮氨酸,必须进行光学异构体的拆分。因此化学合成法很少用于L一亮氨酸的生产。
酶催化法
酶催化法生产L一亮氨酸通常是利用转氨酶转氨给a一酮基异己酸生成L一亮氨酸和组氨酸将相关的酶和NADH共价结合在膜上,让底物缓缓地经过膜而进行酶催化反应生成L一亮氨酸。如1981年,Wichmann er al.建立了一种用超滤膜制成的膜反应器,膜上共价结合了亮氨酸转氨酶、甲酸转氨酶、和NADH,当底物。一酮基异己酸通过膜反应器后,可被催化生成L一亮氨酸,其中NADH通过甲酸同步氧化成C02实现再生。
酶法生产氨基酸的优点是转化能力强,可避免代谢调控中的反馈抑制和反馈阻遏,并且其生物反应器紧凑,产物组分相对单一,易进行后工序加工处理,可以提高产品质量,降低成本。但酶法生产中所用到的酶需通过微生物发酵生成并提取精制,工艺过程比较复杂,且成本较高,因此目前尚未得到广泛的应用。如果能够低成本获得高酶活的酶,则酶法生产L一亮氨酸是一条经济可行的工艺路线。
微生物发酵法
5添加前体物发酵法
1987年德国学者Groegere采用添加前体物。一酮基异己酸生产L一亮氨酸,当培养基中添加前体物。一酮基异己酸的浓度为20g/L,谷氨酸棒杆菌ATCC 13032发酵57h,可生成16g/L L一亮氨酸,质量转化率91-96%;而采用分批流加培养法,可流加a一酮基异己酸32 g/L,发酵23h,产L一亮氨酸24 g/L,从。一酮基异己酸到L一亮氨酸的转化是经过转氨酶的催化生成的。
6用途
亮氨酸生产工艺
一. 浓缩段
原料:蒸汽
将一次母液通入浓缩罐内,通入蒸汽,温度120度,气压-0.09Mpa,浓缩时间6h,结晶。
终点产物:结晶液(去一次中和段)
二,一次中和段
辅料:硫酸,纯水
结晶液进入一次中和罐,通入硫酸,纯水,温度80,中和时间4h,过滤
终点产物:1,滤液(回收利用)2,滤渣(去氨解段)
三, 氨解段
辅料:氨水,纯水,蒸汽
滤渣进入氨解罐,通入氨水,纯水,蒸汽,温度80,氨解时间3h,过滤
终点产物,1,滤液(回收利用)2,滤渣(去脱色段)(胱氨酸)
四,脱色段。
辅料:蒸汽,纯水,活性炭
滤渣进入脱色罐,通(投)入蒸汽,纯水,活性炭,温度80,脱色时间2h,过滤,
终点产物:1,滤渣(回收利用)2,滤液(去二次中和段)
五,二次中和段
辅料:氨水,蒸汽
滤液进入二次中和罐,通入氨水,蒸汽,温度80,中和时间4h,过滤,
终点产物,1,滤液(回收利用)2,滤渣(即L-亮氨酸粗品,去精制段)
六,精制段
辅料:蒸馏水,蒸汽(组氨酸盐酸盐)
用蒸馏水冲洗上段工序产品并离心甩干,送入烘干机,通入蒸汽烘干,包装,入库,烘干温度100,烘干时间3H。
终点产物:L-亮氨酸成品
亮氨酸的作用
亮氨酸的作用包括与异亮氨酸和缬氨酸一起合作修复肌肉,控制血糖,并给身体组织提供能量。它还提高生长激素的产量,并帮助燃烧内脏脂肪,这些脂肪由于处于身体内部,仅通过节食和锻炼难以对它们产生有效作用。
亮氨酸,异亮氨酸和缬氨酸都是支链氨基酸,它们有助于促进训练后的肌肉恢复。其中亮氨酸是最有效的一种支链氨基酸,可以有效防止肌肉损失,因为它能够更快的分解转化为葡萄糖。增加葡萄糖可以防止肌肉组织受损,因此它特别适合健美运动员。白氨酸还促进骨骼,皮肤,以及受损肌肉组织的愈合,医生通常建议手术后患者采取亮氨酸补充剂。
由于它很容易转化为葡萄糖,因此亮氨酸有助于调节血糖水平。白氨酸缺乏的人会出现类似低血糖的症状,如头痛,头晕,疲劳,抑郁,精神错乱,和易怒等。
亮氨酸最好的食物来源包括糙米,豆类,肉类,坚果,大豆粉,和全麦。由于它是一种必不可少的氨基酸,这意味着身体不能自己生产,只能通过饮食获得。从事高强度体力活动和低蛋白质饮食的人,应该考虑采取白氨酸补充。尽管有独立补充形式,但是最好还是与异亮氨酸和缬氨酸一起摄入。因此,选择混合型补充剂更为方便。
但是和任何东西一样,过量摄入亮氨酸也会造成副作用,大量摄入已知与糙皮病,维生素A缺乏症等问题有关系,并会起皮炎,腹泻,精神失常等问题。饮食中含有过多亮氨酸还会增加体内氨的数量,并破坏肝,肾功能。因此,除非咨询过医生,否则肝或肾功能受损患者不应该采用大剂量的亮氨酸,这会导致病情恶化。
2010版中国药典修订增订内容
亮氨酸
Liang’ansuan
Leucine
书页号:2005年版二部-445
[修订]
【检查】 比旋度 取本品,精密称定,用6mol/L盐酸溶液溶解并稀释成每1ml中约含40mg的溶液,依法测定(附录Ⅵ E),比旋度为+14.9°至+16.0°。
其他氨基酸 取本品,用水溶解并制成每1ml中约含20mg的溶液,作为供试品溶液;精密量取供试品溶液适量,用水稀释成每1ml中约含0.1mg的溶液,作为对照溶液;取亮氨酸与缬氨酸对照品各适量,置同一量瓶中,用水溶解并稀释成每1ml中各含0.4mg的混合对照品溶液。照薄层色谱法(附录Ⅴ B)试验,精密吸取上述3种溶液各5µ;l,分别点于同一硅胶G薄层板上,以正丁醇-水-冰醋酸(3:1:1)为展开剂,展开后,晾干,喷以茚三酮的丙酮溶液(1→50),在80℃加热至斑点显色。对照溶液应显一个明显的斑点,混合对照品溶液应显示两个清晰分离的斑点。供试品溶液所显单一杂质斑点的颜色与对照溶液的主斑点比较,不得更深(0.5%)。
7药典2010版
Test Items项目 |
Specification质量指标 |
| Assay,含量 | ≥98,5% |
| Characteristic性状 | White,crystals,or,crystalline,powder,Odorless,slightly,bitter,taste |
| Specific,rotation[a]D比旋度 | +14,9°,~,+15,6° |
| Identification,鉴别 | AS,PER,CP2010 |
| PH酸度 | 5,5~6,5 |
| Transmittance溶液,透光率 | ≥98,0% |
| Chloride,氯化物 | ≤0,02% |
| Sulfate,硫酸盐 | ≤0,02% |
| Ammonium,铵盐 | ≤0,02% |
| Other,amino,acids其他氨基酸 | ≤0,5% |
| Loss,on,drying,干燥失重 | ≤0,2% |
| Residue,on,ignition炽灼残渣 | ≤0,1% |
| Iron,铁盐 | ≤0,001% |
| Heavy,metals(as,Pb)重金属 | ≤10ppm |
| Arsenic砷盐 | ≤0,0001% |
| Bacterial,endotoxins细菌,内毒素 | ≤25,EU/g |
Storage:Preserve in well-closed containers密封保存
